Stories
-
![كأس العالم لكرة القدم]()
كأس العالم لكرة القدم
RT STORIES
القنوات المجانية الناقلة لمباراة مصر والبرازيل الودية استعدادا لكأس العالم 2026
![القنوات المجانية الناقلة لمباراة مصر والبرازيل الودية استعدادا لكأس العالم 2026]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
لمدة 7 ساعات.. تفاصيل احتجاز نجم المنتخب العراقي أيمن حسين في مطار شيكاغو
![لمدة 7 ساعات.. تفاصيل احتجاز نجم المنتخب العراقي أيمن حسين في مطار شيكاغو]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_More![كأس العالم لكرة القدم]() كأس العالم لكرة القدم
كأس العالم لكرة القدم
-
![اتفاق وقف إطلاق النار بين إسرائيل ولبنان]()
اتفاق وقف إطلاق النار بين إسرائيل ولبنان
RT STORIES
"حزب الله": الاتفاق مع إسرائيل عار واستسلام والبعض في لبنان يعاني نقص مناعة وطنية
!["حزب الله": الاتفاق مع إسرائيل عار واستسلام والبعض في لبنان يعاني نقص مناعة وطنية]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
الجيش الإسرائيلي يصدر إنذارا لسكان 5 بلدات لبنانية بإخلائها
![الجيش الإسرائيلي يصدر إنذارا لسكان 5 بلدات لبنانية بإخلائها]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
مقتل ضابط وسائقه استهدفتهما مسيرة إسرائيلية في جنوب لبنان
![مقتل ضابط وسائقه استهدفتهما مسيرة إسرائيلية في جنوب لبنان]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
الجيش الإسرائيلي يعلن عن إصابة ضباط وجنود في مواجهات مع حزب الله في جنوب لبنان
#اسأل_أكثر #Question_MoreRT STORIES
صحيفة إسرائيلية تكشف تفاصيل جديدة عن اغتيال نصر الله: كواليس "دقيقة بدقيقة" في بيروت
![صحيفة إسرائيلية تكشف تفاصيل جديدة عن اغتيال نصر الله: كواليس "دقيقة بدقيقة" في بيروت]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
"حزب الله" ينشر ملخص عملياته ضد إسرائيل الجمعة: تحقيق إصابات مؤكدة وآليات شوهدت تحترق
!["حزب الله" ينشر ملخص عملياته ضد إسرائيل الجمعة: تحقيق إصابات مؤكدة وآليات شوهدت تحترق]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
جنبلاط يحذر من تكرار تجربة أوسلو ومصير فلسطين في المفاوضات مع إسرائيل
![جنبلاط يحذر من تكرار تجربة أوسلو ومصير فلسطين في المفاوضات مع إسرائيل]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
محلّقة انقضاضية تفاجئ الجنود وتنقض عليهم.. مشاهد من عمليات "حزب الله" ضد الجيش الإسرائيلي (فيديو)
![محلّقة انقضاضية تفاجئ الجنود وتنقض عليهم.. مشاهد من عمليات "حزب الله" ضد الجيش الإسرائيلي (فيديو)]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
الجيش الإسرائيلي يعلن اغتيال قائد وحدة الهندسة في "حزب الله" وتدمير منصة صاروخية
![الجيش الإسرائيلي يعلن اغتيال قائد وحدة الهندسة في "حزب الله" وتدمير منصة صاروخية]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
وسائل إعلام: نتنياهو تعرض لأضرار سياسية بسبب تسريب محادثته مع ترامب
![وسائل إعلام: نتنياهو تعرض لأضرار سياسية بسبب تسريب محادثته مع ترامب]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
عون يوجه رسائل نارية لإيران و"حزب الله": نعيم قاسم لا يمثل شعبنا ولبنان ليس ساحة لمصالحكم
![عون يوجه رسائل نارية لإيران و"حزب الله": نعيم قاسم لا يمثل شعبنا ولبنان ليس ساحة لمصالحكم]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_More![اتفاق وقف إطلاق النار بين إسرائيل ولبنان]() اتفاق وقف إطلاق النار بين إسرائيل ولبنان
اتفاق وقف إطلاق النار بين إسرائيل ولبنان
-
![هدنة وحصار المضيق]()
هدنة وحصار المضيق
RT STORIES
المنامة تضع أمام طهران خيارين لا ثالث لهما وتذكرها بخط أحمر بعد هجماتها الجديدة على البحرين والكويت
![المنامة تضع أمام طهران خيارين لا ثالث لهما وتذكرها بخط أحمر بعد هجماتها الجديدة على البحرين والكويت]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
مجلة عسكرية: خروج مركز العمليات الجوية الأمريكية في قاعدة العديد بقطر عن الخدمة
![مجلة عسكرية: خروج مركز العمليات الجوية الأمريكية في قاعدة العديد بقطر عن الخدمة]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
"ترامب سيرحل".. سياسي إيراني يقترح حلا لأزمة البرنامج النووي
!["ترامب سيرحل".. سياسي إيراني يقترح حلا لأزمة البرنامج النووي]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
الحرس الثوري الإيراني: قصفنا قاعدة علي السالم بالكويت والأسطول الخامس بالبحرين
![الحرس الثوري الإيراني: قصفنا قاعدة علي السالم بالكويت والأسطول الخامس بالبحرين]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
إنذارات بهجمات صاروخية ومسيرات معادية في الكويت والبحرين (فيديوهات)
![إنذارات بهجمات صاروخية ومسيرات معادية في الكويت والبحرين (فيديوهات)]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
مبعوثا ترامب إلى إيران يجريان محادثات سرية مع خبراء نوويين في تينيسي
![مبعوثا ترامب إلى إيران يجريان محادثات سرية مع خبراء نوويين في تينيسي]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
ترامب: نحقق نجاحا باهرا مع إيران
![ترامب: نحقق نجاحا باهرا مع إيران]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
ترامب يهدد باستئناف القتال ضد إيران ويعلن: لم يتبق لديها سوى 22% من صواريخها
![ترامب يهدد باستئناف القتال ضد إيران ويعلن: لم يتبق لديها سوى 22% من صواريخها]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
القيادة المركزية الأمريكية: إسقاط 4 مسيرات إيرانية قرب مضيق هرمز واستهداف مواقع رادار إيرانية
![القيادة المركزية الأمريكية: إسقاط 4 مسيرات إيرانية قرب مضيق هرمز واستهداف مواقع رادار إيرانية]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
مهر: سماع دوي انفجارات في منطقة ميناء سيريك جنوب إيران
![مهر: سماع دوي انفجارات في منطقة ميناء سيريك جنوب إيران]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
إيران تهدد ترامب بحرب تمتد من هرمز إلى المحيط الهندي ومضيق باب المندب والبحرين الأحمر والمتوسط
![إيران تهدد ترامب بحرب تمتد من هرمز إلى المحيط الهندي ومضيق باب المندب والبحرين الأحمر والمتوسط]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
مستشار خامنئي: لقاء ترامب والمرشد الأعلى لإيران غير ممكن حاليا
![مستشار خامنئي: لقاء ترامب والمرشد الأعلى لإيران غير ممكن حاليا]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
إيران تطلب الإفراج عن أصول بقيمة 24 مليار دولار لإبرام صفقة مع أمريكا
![إيران تطلب الإفراج عن أصول بقيمة 24 مليار دولار لإبرام صفقة مع أمريكا]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_More![هدنة وحصار المضيق]() هدنة وحصار المضيق
هدنة وحصار المضيق
-
![مونديال 2026]()
مونديال 2026
RT STORIES
فنان أمريكي يقاضي "فيفا" ويطالب بـ25 مليون دولار
![فنان أمريكي يقاضي "فيفا" ويطالب بـ25 مليون دولار]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
كيف تشاهد مونديال 2026؟.. تفاصيل القنوات الناقلة ومواعيد مباريات الفرق العربية
![كيف تشاهد مونديال 2026؟.. تفاصيل القنوات الناقلة ومواعيد مباريات الفرق العربية]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
كرة المونديال تتسبب في لقطة طريفة خلال مؤتمر رئيسة المكسيك (فيديو)
![كرة المونديال تتسبب في لقطة طريفة خلال مؤتمر رئيسة المكسيك (فيديو)]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
دراسة تتوقع المرشح الأبرز لنيل لقب كأس العالم 2026
#اسأل_أكثر #Question_More![مونديال 2026]() مونديال 2026
مونديال 2026
-
![منتدى بطرسبورغ الاقتصادي الدولي]()
منتدى بطرسبورغ الاقتصادي الدولي
RT STORIES
نائب أوروبي يطالب بحرمان دول البلطيق من حماية "الناتو" جراء استفزازاتها ضد روسيا
![نائب أوروبي يطالب بحرمان دول البلطيق من حماية "الناتو" جراء استفزازاتها ضد روسيا]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
بوتين: إيران لم ترتكب استفزازات تبرر الهجوم الأمريكي ونأمل بهدنة تفضي إلى سلام دائم
![بوتين: إيران لم ترتكب استفزازات تبرر الهجوم الأمريكي ونأمل بهدنة تفضي إلى سلام دائم]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
بوتين: أساليب الحرب تتغير باستمرار وروسيا تعزز دفاعاتها الجوية وتحتفظ بأسلحة لا تملكها دول أخرى
![بوتين: أساليب الحرب تتغير باستمرار وروسيا تعزز دفاعاتها الجوية وتحتفظ بأسلحة لا تملكها دول أخرى]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
رئيس الوفد الأمريكي في منتدى بطرسبورغ: أشكر بوتين على كرم الضيافة وأحب هذه المدينة كثيرا
![رئيس الوفد الأمريكي في منتدى بطرسبورغ: أشكر بوتين على كرم الضيافة وأحب هذه المدينة كثيرا]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
بوتين: روسيا ستسعى لتحقيق هدف اجتثاث النازية من أوكرانيا عبر المفاوضات
![بوتين: روسيا ستسعى لتحقيق هدف اجتثاث النازية من أوكرانيا عبر المفاوضات]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
بوتين: الدول الغربية أطلقت عملية تآكل منظمة التجارة العالمية
![بوتين: الدول الغربية أطلقت عملية تآكل منظمة التجارة العالمية]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
بوتين: استخدام الدولار كسلاح سياسي "خطأ استراتيجي فادح"
![بوتين: استخدام الدولار كسلاح سياسي "خطأ استراتيجي فادح"]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
"شراكة استراتيجية حقيقية".. روسيا والسعودية توقعان 30 اتفاقية في منتدى بطرسبورغ الاقتصادي (فيديو)
!["شراكة استراتيجية حقيقية".. روسيا والسعودية توقعان 30 اتفاقية في منتدى بطرسبورغ الاقتصادي (فيديو)]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
وزير الصناعة السعودي يزور جناح RT في منتدى بطرسبورغ الدولي (فيديو)
![وزير الصناعة السعودي يزور جناح RT في منتدى بطرسبورغ الدولي (فيديو)]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
"العالم يشهد تحولا هيكليا كبيرا".. أبرز تصريحات بوتين أمام منتدى بطرسبورغ
!["العالم يشهد تحولا هيكليا كبيرا".. أبرز تصريحات بوتين أمام منتدى بطرسبورغ]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
دميترييف يكشف عن سلاح روسيا التنافسي في سباق الذكاء الاصطناعي العالمي
![دميترييف يكشف عن سلاح روسيا التنافسي في سباق الذكاء الاصطناعي العالمي]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
وزير الطاقة السعودي يزور أجنحة منتدى بطرسبورغ الاقتصادي
![وزير الطاقة السعودي يزور أجنحة منتدى بطرسبورغ الاقتصادي]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
شاهد.. الأمير عبد العزيز يتلقى هدايا تذكارية على هامش منتدى بطرسبورغ
![شاهد.. الأمير عبد العزيز يتلقى هدايا تذكارية على هامش منتدى بطرسبورغ]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_More![منتدى بطرسبورغ الاقتصادي الدولي]() منتدى بطرسبورغ الاقتصادي الدولي
منتدى بطرسبورغ الاقتصادي الدولي
-
![العملية العسكرية الروسية في أوكرانيا]()
العملية العسكرية الروسية في أوكرانيا
RT STORIES
إسقاط 25 مسيرة في مقاطعة لينينغراد الروسية
![إسقاط 25 مسيرة في مقاطعة لينينغراد الروسية]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
بوتين: كييف تريد وقف تقدم قواتنا ونحن مستعدون لاتفاقيات طويلة الأمد
![بوتين: كييف تريد وقف تقدم قواتنا ونحن مستعدون لاتفاقيات طويلة الأمد]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
أوشاكوف: بوتين أجري محادثة ودية مع المستشار الألماني الأسبق شرودر في الكرملين
![أوشاكوف: بوتين أجري محادثة ودية مع المستشار الألماني الأسبق شرودر في الكرملين]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
إعلام: زيلينسكي يريد مناقشة مفاوضات محتملة مع روسيا مع شركائه
![إعلام: زيلينسكي يريد مناقشة مفاوضات محتملة مع روسيا مع شركائه]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
وزارة الدفاع الروسية تستجيب لتوجيهات بوتين (صورة)
![وزارة الدفاع الروسية تستجيب لتوجيهات بوتين (صورة)]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
بوتين يشيد بترامب ويهاجم زيلينسكي: يريد السلاح الأمريكي ويرفض واشنطن ضامنا للتسوية
![بوتين يشيد بترامب ويهاجم زيلينسكي: يريد السلاح الأمريكي ويرفض واشنطن ضامنا للتسوية]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
أوشاكوف: الاتصالات مستمرة مع ويتكوف وكوشنر وزيارتهما لروسيا "قيد التحضير"
![أوشاكوف: الاتصالات مستمرة مع ويتكوف وكوشنر وزيارتهما لروسيا "قيد التحضير"]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
بيسكوف يرفض الكشف عن رد بوتين على رسالة زيلينسكي
![بيسكوف يرفض الكشف عن رد بوتين على رسالة زيلينسكي]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
ماكرون: رسالة زيلينيسكي إلى بوتين مبادرة جيدة وحان وقت الحوار مع روسيا
![ماكرون: رسالة زيلينيسكي إلى بوتين مبادرة جيدة وحان وقت الحوار مع روسيا]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
لافروف: لم نتسلم رسالة زيلينسكي عبر القنوات الرسمية
![لافروف: لم نتسلم رسالة زيلينسكي عبر القنوات الرسمية]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_More![العملية العسكرية الروسية في أوكرانيا]() العملية العسكرية الروسية في أوكرانيا
العملية العسكرية الروسية في أوكرانيا
-
![فيديوهات]()
فيديوهات
RT STORIES
الجيش اللبناني يدخل إلى بلدة دبين في قضاء مرجعيون
![الجيش اللبناني يدخل إلى بلدة دبين في قضاء مرجعيون]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
لحظة استهداف مسيرة انتحارية أوكرانية لميناء في رومانيا
![لحظة استهداف مسيرة انتحارية أوكرانية لميناء في رومانيا]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
رصد ترامب وهو يأخذ قيلولة بعد يوم من الخلاف في الكونغرس حول نومه أثناء الاجتماعات
![رصد ترامب وهو يأخذ قيلولة بعد يوم من الخلاف في الكونغرس حول نومه أثناء الاجتماعات]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
دقائق معدودة فصلت تبينه وبين الرسوب.. شرطة دمشق تنقذ طالبا من تأخير الامتحان
![دقائق معدودة فصلت تبينه وبين الرسوب.. شرطة دمشق تنقذ طالبا من تأخير الامتحان]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
العراق.. إنزال راية "سرايا السلام" في سامراء أثناء مراسم تسليم أسلحتها للدولة
![العراق.. إنزال راية "سرايا السلام" في سامراء أثناء مراسم تسليم أسلحتها للدولة]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
لغز غريب في نيويورك.. اختفاء أشخاص داخل المجاري وسط الليل يحير السكان والشرطة تحقق
![لغز غريب في نيويورك.. اختفاء أشخاص داخل المجاري وسط الليل يحير السكان والشرطة تحقق]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
الجيش الأمريكي يستهدف قاربا جديدا في المحيط الهادئ
![الجيش الأمريكي يستهدف قاربا جديدا في المحيط الهادئ]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
وزير الطاقة السعودي يزور منتدى بطرسبورغ الاقتصادي الدولي
![وزير الطاقة السعودي يزور منتدى بطرسبورغ الاقتصادي الدولي]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_MoreRT STORIES
قطع كلمة روبيو بسبب "خدمة" إسرائيل خلال جلسة استماع أمام مجلس الشيوخ
![قطع كلمة روبيو بسبب "خدمة" إسرائيل خلال جلسة استماع أمام مجلس الشيوخ]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_More![فيديوهات]() فيديوهات
فيديوهات
-
![عملاق إيطالي يدخل خط المنافسة ويتحرك لضم محمد صلاح]()
عملاق إيطالي يدخل خط المنافسة ويتحرك لضم محمد صلاح
RT STORIES
عملاق إيطالي يدخل خط المنافسة ويتحرك لضم محمد صلاح
![عملاق إيطالي يدخل خط المنافسة ويتحرك لضم محمد صلاح]() #اسأل_أكثر #Question_More
#اسأل_أكثر #Question_More
الكشف عن أول ملاحظة على الإطلاق لبنية بروتينات ألزهايمر في الدماغ
رصد العلماء لأول مرة، تركيب كتل البروتين المرتبطة بمرض ألزهايمر، وكيف تتشكل في أدمغة المرضى.

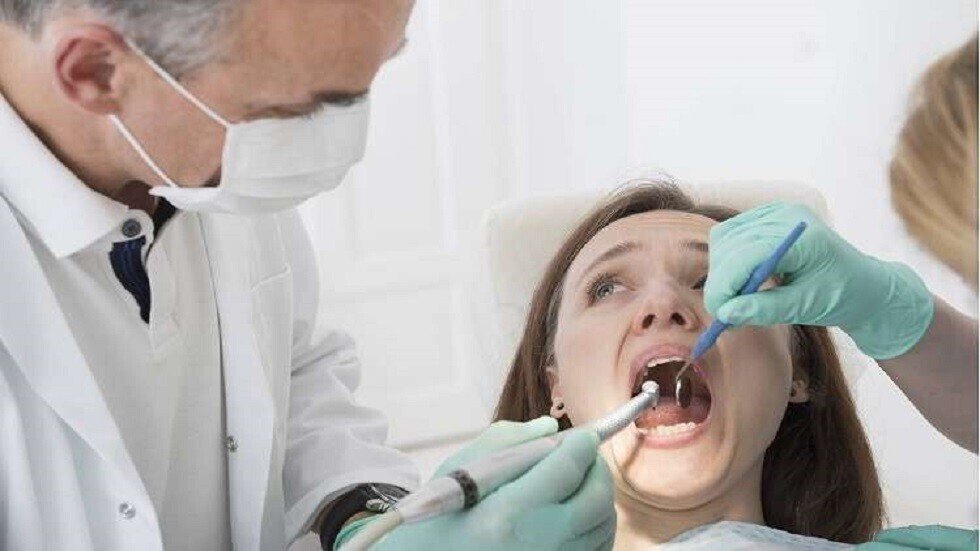
أعراض تظهر في الفم قد تكون علامات تحذيرية للإصابة بأزمة قلبية
وتمكن العلماء من استخلاص وعزل ألياف أميلويد بيتا (Aβ) من أدمغة ثلاثة أشخاص توفوا بسبب مرض ألزهايمر، ثم قاموا بتحليل هذه المجموعات البروتينية لتحديد تفاصيل تركيبتها.
واستخدم الفريق، الذي شمل علماء من جامعة كوينزلاند في أستراليا وعلماء من جامعة أولم في ألمانيا، المجهر الإلكتروني لإلقاء نظرة فاحصة على الألياف، واكتشف أنها بنيت بشكل مختلف تماما عن البروتينات التي يمكن إنتاجها في المختبر.
وهذه التركيبة السامة من البروتينات تقتل الخلايا القريبة، لكن من غير الواضح كيف تتجمع مع بعضها أو لماذا لا يتخلص منها الجسم.
ويمكن لمعرفة المزيد حول كيفية بناء هذه الألياف أن يساعد العلماء في حل هذه الألغاز. وأشار الفريق إلى أن "الهيكل المرصود يختلف اختلافا كبيرا عن الهياكل المعروفة من التكتلات الليفية لأميلويد بيتا التي يتم تشكيلها في المختبر".
The cryo-EM structure of patient derived Aβ amyloid fibrils was solved by the lab of Prof. Marcus Fändrich and their collaborators.@DZNE_de @uni_ulmhttps://t.co/wqsaXDo8u2 pic.twitter.com/ntbNRYoGcD
— Nature Communications (@NatureComms) October 31, 2019
Cryo-EM structure and polymorphism of Aβ amyloid fibrils purified from Alzheimer’s brain tissue https://t.co/2gvhJs0jEx pic.twitter.com/ENhbaot1O8
— Krishan Maggon (@kkmaggon) October 30, 2019
وتشير الدراسة إلى أنه إذا وجد العلماء أدوية قادرة على تنظيف الدماغ من تكتلات بروتينات الأميلويد بيتا، فلا يأتي اختبارها على التكتلات الليفية التي أنتجت في أنابيب الاختبارات، لأن ما يحدث داخل أدمغة المصابين بمرض ألزهايمر، قد يكون مختلفا تماما.
https://t.co/JURg90vcj7 Cryo-EM structure and polymorphism of Aβ amyloid fibrils purified from Alzheimer’s brain tissue
— Druse Labs (@druselabs1) October 29, 2019
by
Marius Kollmer
William Close
Leonie Funk
Jay Rasmussen
Aref Bsoul
Angelika Schierhorn
Matthias Schmidt
Christina Sigurdson
Mathias Jucker
Marcus Fändrich pic.twitter.com/pjeru0jWyO
وأفاد العلماء بأن الطريقة التي يتم بها طي البروتينات في الدماغ، لم تكن ذاتها التي تم رصدها في السابق في النماذج المختبرية، حيث رصدوا تطورا للتكتلات الليفية لأميلويد بيتا في الجانب الأيمن بدلا من اليسار.
كما وجد العلماء اختلافات هيكلية بين الألياف أيضا، ما يؤكد الحاجة إلى اتباع نهج شخصي لكل حالة عند علاج ألزهايمر.
Cryo-EM structure and polymorphism of Aβ amyloid fibrils purified from Alzheimer’s #brain tissue https://t.co/1YdZPYMM96 @NatureComms pic.twitter.com/vu6hKOREGn
— Behav Ecol Papers (@BehavEcolPapers) October 29, 2019
ورصد الفريق هذه الاختلافات في الألياف في أدمغة العينات الثلاثة، لكنه لا يستبعد إمكانية العثور على المزيد من الاختلافات لدى مرضى آخرين.

أنماط النوم تقدم مفتاح التشخيص المبكر لمرض ألزهايمر
وفي حين ما تزال هناك بعض الثغرات في فهم هيكل التكتلات الليفية لأميلويد بيتا، تعد هذه الدراسة خطوة مفيدة إلى الأمام في معرفة ما الذي يتعامل معه العلماء بالتحديد عندما يتعلق الأمر بمرض ألزهايمر وطريقة انسداد الدماغ.
وأشارت الأبحاث الحديثة إلى أن مرض ألزهايمر قد يكون له أصل بكتيري، وهو نوع من العدوى نلتقطها بطريقة أو بأخرى عندما تتعطل أنظمة الدفاع عن النفس في أجسامنا عن العمل، ولكن ما يزال هناك الكثير من الأسئلة التي ينبغي الإجابة عنها حول هذا المرض.
وخلص العلماء في هذه الدراسة إلى أن نتيجة هذه الملاحظات تكمن في أن استهداف مورفولوجيا (شكل وهيكل) ليفية محددة بمثبطات انتقائية مناسبة قد يمثل استراتيجية هامة في التدخلات العلاجية للمرض.
المصدر: ساينس ألرت








































































































































































التعليقات